Елена Бабичева
Не лучший хирург: как нобелевский лауреат Синъя Яманака заложил будущее медицины
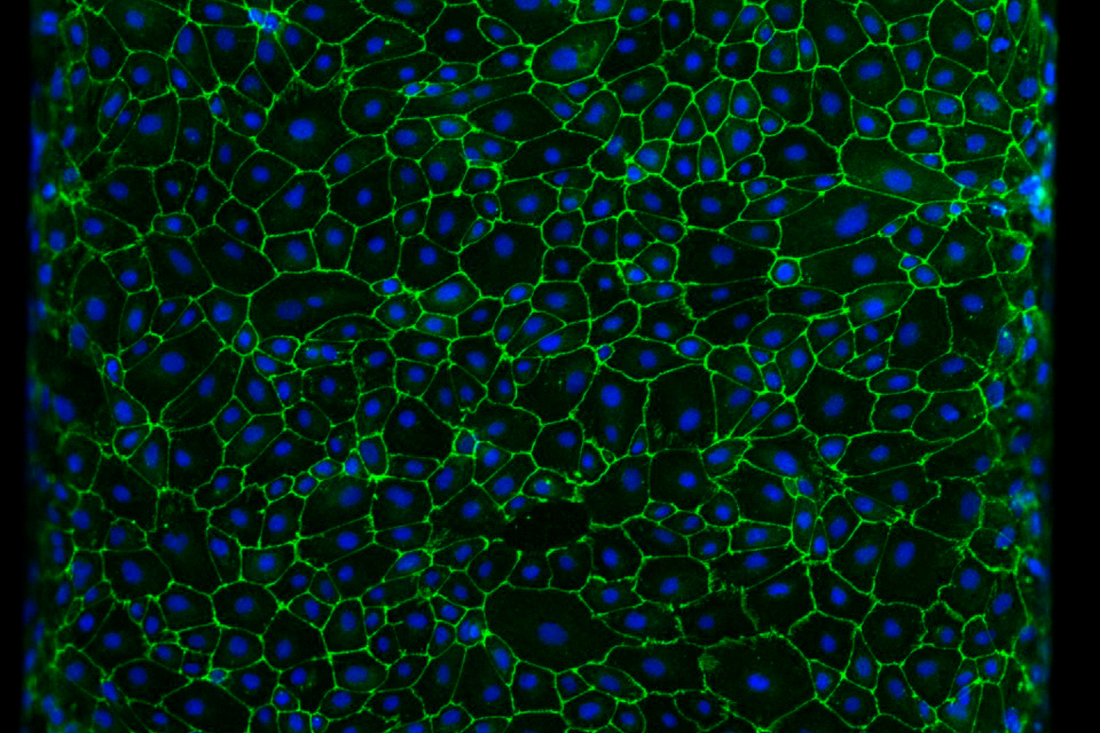
Возможность получить плюрипотентные стволовые клетки, которые являются родоначальниками практически всех тканей и органов, путем перепрограммирования взрослых соматических клеток, а не эмбриональных стала настоящим прорывом. Их открытие решает массу медицинских и этических проблем. А совершил этот прорыв японский ученый Синъя Яманака.
В детстве Синъя Яманака хотел стать инженером, как и его отец. Тот владел небольшой компанией: конструировал разные товары, сам производил их и продавал. Подражая отцу, Яманака часто сидел за чертежами, хотя больше любил разбирать и заново собирать радиоприемники и часы. А еще ему нравились математика и физика, так что вполне естественно, что молодой человек решил изучать фундаментальные науки.
Выбор пал на медицину. С одной стороны, это посоветовал отец, который считал работу врача более стабильной, чем бизнес. С другой — сам юный Яманака хотел приносить пользу людям. Во время учебы в университете он определился и со специальностью хирурга-ортопеда. И неслучайно. Будучи заядлым игроком в регби, Яманака перенес несколько переломов, страдал от постоянных болей в ногах. Этот опыт пробудил в нем интерес к спортивной медицине.
Яманака работал в Национальной больнице Осаки, проводил операции, занимался лечением травм. Но чувствовал, что блестящий хирург из него не получится, а посредственным быть не хотелось. «Однажды мне потребовалось два часа, чтобы сделать хирургическую операцию, которую другие хирурги могли бы сделать за 30 минут», — годы спустя признавался он в интервью.
А главное, молодой врач вдруг осознал, что даже самым талантливым хирургам подчас не под силу вылечить какие-то заболевания. Те методы, которые существуют, не всегда помогают.
Яманака ушел из больницы, решив учиться дальше, чтобы понять, чем именно он хочет заниматься, какие исследования проводить.
Пробуждение амбиций

Окончательный поворот в сторону фундаментальной науки произошел благодаря, казалось бы, незначительному случаю. Яманака работал в лаборатории у своего наставника Кацуюки Миуры и изучал роль липидов, которые являются фактором активации тромбоцитов в снижении давления — исследование велось на собаках. Вопреки гипотезе Миуры введение конкретных липидов не предотвратило снижение давления.
В общем-то, рядовое событие: сплошь и рядом научные гипотезы не подтверждаются, а проводимые эксперименты опровергают их. И приходится вновь и вновь задавать вопросы и искать на них ответы. Но необходимость поиска решений взволновала и покорила молодого доктора, а возможность конкурировать с выдающимися исследователями пробудила честолюбивые замыслы.
В 1993 году Яманака уезжает в США на работу в Гладстонский институт сердечно-сосудистых заболеваний в Сан-Франциско, где начинает исследовать ген с-MYC у различных линий специфических мышей — так называемых нокаутных, то есть с определенным геном.
Через полтора десятка лет ген с-MYC станет одним из четырех «ингредиентов» ставшего знаменитым «коктейля Яманаки».
А пока молодой ученый продолжал изучать молекулярные механизмы онкогенеза (процесса возникновения злокачественных новообразований), учиться у коллег культивировать эмбриональные стволовые клетки мыши и создавать химеры.
До сих пор, по признанию самого Яманаки, ту работу он считает идеальной с точки зрения условий для проведения исследований, возможности вести постоянные научные дискуссии с такими же увлеченными коллегами. И главное, она помогла ему определить цель своей научной деятельности.
— Однажды Роберт Мали, тогдашний президент Гладстона, собрал около 20 постдоков и сказал, что «фольксваген» — это волшебное слово, которое сделает нас успешными учеными. Он имел в виду, что ученые должны иметь четкое видение и усердно работать над его достижением. У меня не было ясного видения, хотя я был уверен, что в то время был одним из самых трудолюбивых постдоков в Гладстоне.

С тех пор я определил свое видение таким образом: способствовать разработке новых лекарств для пациентов с помощью фундаментальных исследований, — рассказывал о том периоде Яманака, выступая с речью по случаю вручения ему Нобелевской премии в 2012 году.
Тьма и свет
Через несколько лет Яманака вернулся в Японию, где продолжил изучать нокаутные гены, в частности NAT1, и их функцию у мышей. В ходе экспериментов ученый обнаружил, что эмбриональные стволовые клетки, не содержащие этот ген, не могут должным образом дифференцироваться. Это неожиданное открытие превратило мышиные эмбриональные стволовые клетки из инструмента исследования в его предмет: как-то же они сохраняют свою способность к дифференцировке при быстром размножении.
До главного открытия ученого оставалось еще десять лет. И как сгущается тьма перед рассветом, так и перед прорывом наступило непростое время.
Научная среда в Японии существенно отличалась от американской. Яманаке не хватало увлеченных дискуссий и пищи для размышлений. Японские коллеги не разделяли его научных интересов к биологии эмбриональных стволовых клеток, кроме того, многие советовали ему заняться чем-то более приближенным к медицине. Финансирование для экспериментов было недостаточным, а несколько научных журналов отвергли его статью о NAT1.
Яманака уже всерьез подумывал о том, чтобы вернуться к карьере врача… Но тут случились знаковые перемены.
На исходе ХХ века Джеймс Томсон из Университета Висконсин-Мэдисон (США) и его коллеги объявили, что им удалось получить человеческие эмбриональные стволовые клетки.
Это открытие было дополнительным аргументом в пользу того, что эти клетки обладают огромным потенциалом для медицины. Оно вдохновило Яманаку на продолжение работы. К тому же подоспело еще одно благоприятное событие: он наконец получил собственную лабораторию в Институте науки и технологии Нары для исследования нокаутных мышей.
На пути к прорыву
Успешное получение эмбриональных стволовых (ЭС) клеток у человека вызвало в научном сообществе небывалый интерес к ним. Перед наукой встала новая задача — научиться дифференцировать их в соматические. Решение задачи было сопряжено с этическими препятствиями, ведь для дальнейших исследований требовалось использовать человеческие эмбрионы, что запрещалось и в Японии, и в США. Существовало препятствие и медицинского порядка: трансплантация этих клеток неизменно вызывала иммунное отторжение.
Чтобы обойти эти проблемы, Яманака решает сосредоточиться на ядерном перепрограммировании. Начало ему положил еще британский биолог Джон Гердон. Тогда, в 1962 году, Яманака только родился, а Гердон уже сумел вывести новых лягушек путем переноса ядер клеток кишечника головастика в энуклеированные (с удаленным ядром) яйца африканской когтистой жабы. Спустя 30 лет подобный эксперимент ученым удалось провести на млекопитающем — так в 1997 году появилась овечка Долли.
Эти достижения показали, что геномная ДНК зрелых клеток теоретически обладает всей информацией, необходимой для развития животных. Вскоре стало ясно, что основные этапы дифференцировки начинаются в тимусе, в который из костного мозга мигрируют ранние предшественники Т-лимфоцитов, и при слиянии с ЭС клетками мыши они приобретают плюрипотентность — способность дифференцироваться в клетки разных тканей и органов. Это означало, что теми же способностями обладают и ЭС клетки. Оставалось лишь определить факторы, которые ведут к индуцированию плюрипотентности соматических клеток.

В результате исследований был найден еще один ген — фактор транскрипции KLF4, идентифицированный одним из сотрудников лаборатории. А к 2004 году команда представила 24 исходных гена-кандидата, которые могли бы индуцировать плюрипотентность в соматических клетках.
Вместе с этим багажом — генами, подопытными нокаутными мышами — и несколькими коллегами Яманака переводится в Киотский университет, чтобы продолжить исследования с использованием человеческих ЭС клеток. Культивировать их удалось лишь Киотскому университету.
Начало без конца
Прежде чем ученый воскликнет «Эврика!», ему предстоит долгий кропотливый труд. В данном случае необходимо было ввести каждый ген-кандидат в определенные мышиные фибробласты и затем наблюдать, что происходит. А происходило удивительное: некоторые полученные клетки оказались схожи с эмбриональными стволовыми по нескольким характеристикам: по морфологии, пролиферации и экспрессии генов.
Когда мышам пересадили эти клетки, в них образовывались тератомы (вид опухоли), содержащие разнообразные ткани из всех трех зародышевых листков, демонстрирующие их плюрипотентность. При пристальном изучении выяснилось, что к подобному результату приводили четыре гена — так называемые факторы транскрипции OCT-¾, SOX2 и уже известные KLF4 и c-MYC. Именно эти четыре гена играли главную роль в образовании тератом.
Полученные путем перепрограммирования эмбриональные стволовые клетки Яманака назвал индуцированными.
Несмотря на успешные опыты, Яманака беспокоился за точность эксперимента. Слишком уж просто все оказалось.
Как впоследствии признавался ученый, он думал, что путь будет долгим, и не был уверен, что достигнет цели еще при своей жизни. Поэтому со своей научной группой он повторяет эксперимент еще раз, чтобы убедиться, что для перепрограммирования соматических клеток в эмбриональное состояние действительно требуется всего четыре гена, которые превращают их в плюрипотентные.
В ноябре 2007 года команда Яманаки сообщила о получении индуцированных стволовых клеток из человеческих фибробластов путем введения все того же квартета генов с помощью вирусных векторов. Почти одновременно с Яманакой о создании индуцированных стволовых клеток объявила и лаборатория Томсона — они использовали другой набор из четырех факторов: NANOG, LIN28, OCT¾ и SOX2.
Не собираясь останавливаться на достигнутом, сотрудники лаборатории Яманаки продолжали совершенствовать методы индукции и отбора. Кейсуке Оките удалось создать индуцированные стволовые клетки, способные производить взрослые химеры. Масато Накагава и Митие Коянаги показали, что эти клетки могут быть получены без онкогена c-MYC. А Такаси Аои доказал, что их можно получить не только из фибробластов, но также из гепатоцитов взрослых мышей и эпителиальных клеток желудка.
Сегодня технологии получения индуцированных стволовых клеток развиваются с невероятной скоростью.
Созданы протоколы для прямого перепрограммирования, посредством которых соматические клетки напрямую превращаются в зрелые клетки другого типа. А лаборатория Яманаки разработала метод получения индуцированных стволовых клеток без интеграции вирусных векторов в клеточный геном, что делает метод более безопасным.
Сейчас его команда работает над проектом по созданию линии индуцированных стволовых клеток из донорских клеток крови. Полученные линии будут переданы другим институтам, чтобы те могли дифференцировать их в различные типы клеток для использования в трансплантационной терапии.
В 2012 году за свое открытие Синъя Яманака получил Нобелевскую премию. На ее вручении он сказал: «Хотя я отказался от карьеры хирурга, я все еще надеюсь помочь людям, страдающим от тяжелых заболеваний и травм».