Татьяна Маринович
Ученые выяснили причину развития миелофиброза
Виной тому нарушение механических свойств костного мозга
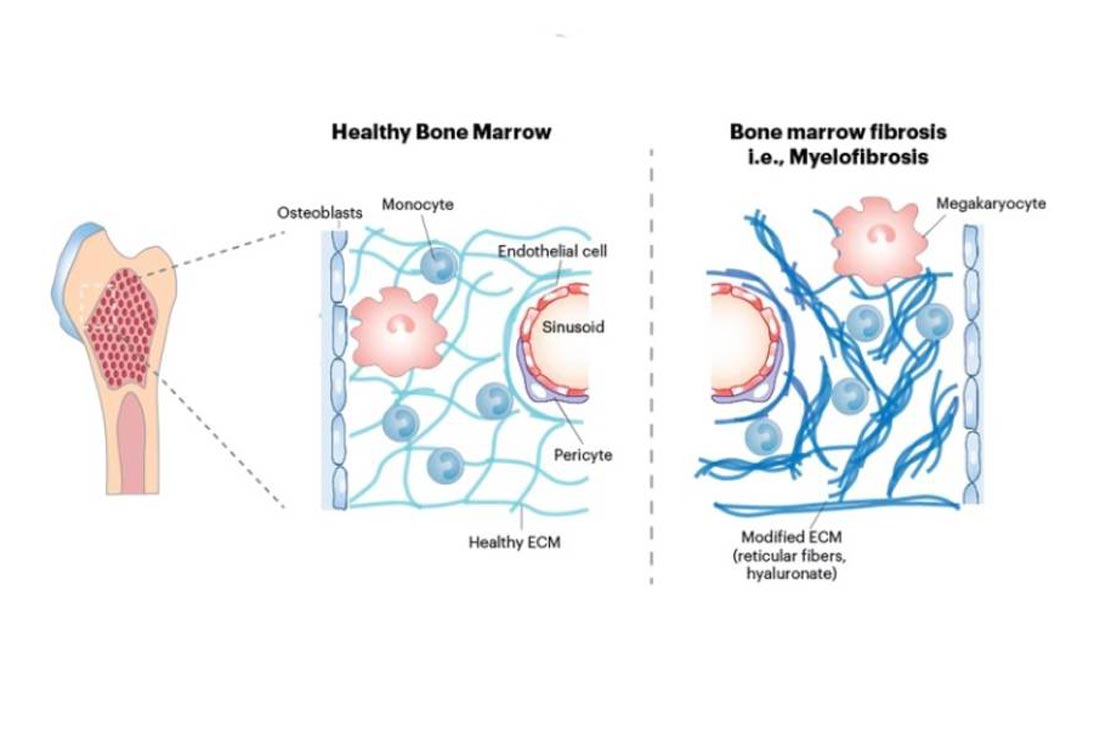
Миелофиброз – хроническое заболевание крови, при котором костный мозг постепенно замещается опухолевыми клетками и соединительной тканью, а в тяжелых случаях перерастает в острый лейкоз. Почему он развивается, прежде точно было неизвестно.
В принципе фиброз, то есть утолщение тканей, может возникать при заживлении ран и других повреждений. Однако, если он сопровождается воспалением или приемом вредных веществ, это приводит к заболеваниям органов. Так, курение может вести к фиброзу легких, злоупотребление алкоголем – к фиброзу печени. В случае фиброза костного мозга клетки крови не созревают до конца, образуются тромбы.
Среди возможных причин развития миелофиброза рассматривались генетические мутации, сопутствующие вирусные инфекции (например, вирус простого герпеса, вирус Эпштейна – Барр), контакт с токсинами вроде мышьяка и бензола и даже радиация.
Недавнее исследование американских ученых показало, как действует механизм ракового перерождения клеток при миелофиброзе. Команда ученых из гарвардского Института биоинженерии Висса, Гарвардской школы инженерных и прикладных наук Джона А. Полсона, Института рака Дана – Фарбер и Женской больницы Бригама создали лабораторную гидрогелевую модель, имитирующую здоровый и фиброзный костный мозг человека, и сопоставили ее действие с миелофиброзом у мышей.
Исследователи выяснили, что иммунные клетки переходят в воспалительное состояние из-за механических свойств ниш стволовых клеток – особого микроокружения из поддерживающих клеток и внеклеточного матрикса.
О каких механических свойствах идет речь? Ниша стволовых клеток в здоровом состоянии вязкая и в то же время эластичная. При деформации, давлении или растяжении она быстро возвращает себе исходное состояние.
Гидрогелевая модель помогла воспроизвести эти свойства в здоровом костном мозге и пораженном фиброзом. Ученые выяснили, что моноциты (один из видов иммунных клеток) человека, помещенные в искусственную нишу стволовых клеток, могут реагировать на ее механические характеристики. Так, незрелые моноциты в искусственной имитации фиброзной ниши, которая отличается большей жесткостью, запускали воспалительный процесс, похожий на таковой у пациентов с миелофиброзом. Более вязкие же среды подавляли этот эффект.
Ученые сделали вывод, что именно нарушенные механические свойства костного мозга вызывают миелофиброз. Серия последующих экспериментов показала, что степень патологического перерождения иммунных клеток напрямую зависит от изменения вязкости и упругости среды.
В настоящее время эффективных методик лечения миелофиброза нет. В борьбе с ним применяют пересадку костного мозга.
Можно ли на основе сделанного открытия разработать новую действенную терапию? Некоторые экспериментальные успехи в этом направлении уже есть. Исследователи обратили внимание на особый белок PI3K Gamma, который выделяется в моноцитах и регулирует подвижность, форму и рост клеток. В ответ на механическое давление ниши костного мозга этот белок заставляет клетки избыточно расти, приводя к фиброзу. Препарат, который подавлял действие белка в жесткой искусственной нише, помог снять воспаление.
Результаты данного исследования позволяют взглянуть на функции иммунных клеток по-новому и в перспективе разработать действенные способы борьбы с раковыми фиброзными заболеваниями.
Спасибо за ваше внимание! Уделите нам, пожалуйста, еще немного времени. Кровь5 — издание Русфонда, и вместе мы работаем для того, чтобы регистр доноров костного мозга пополнялся новыми участниками и у каждого пациента с онкогематологическим диагнозом было больше шансов на спасение. Присоединяйтесь к нам: оформите ежемесячное пожертвование прямо на нашем сайте на любую сумму — 500, 1000, 2000 рублей — или сделайте разовый взнос на развитие Национального регистра доноров костного мозга имени Васи Перевощикова. Помогите нам помогать. Вместе мы сила.
Ваша,
Кровь5